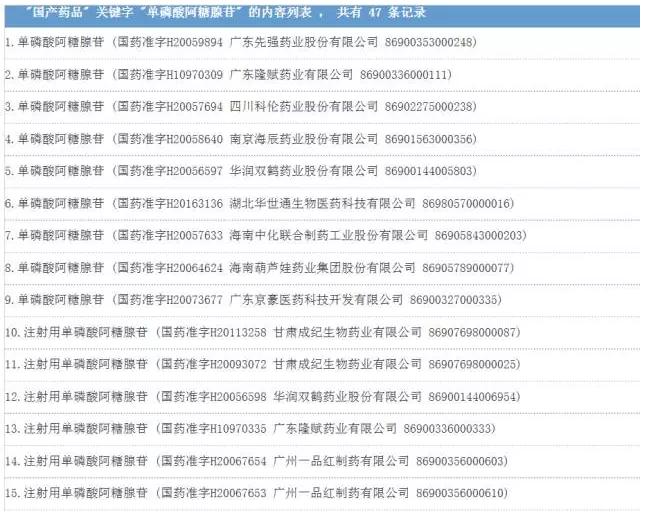
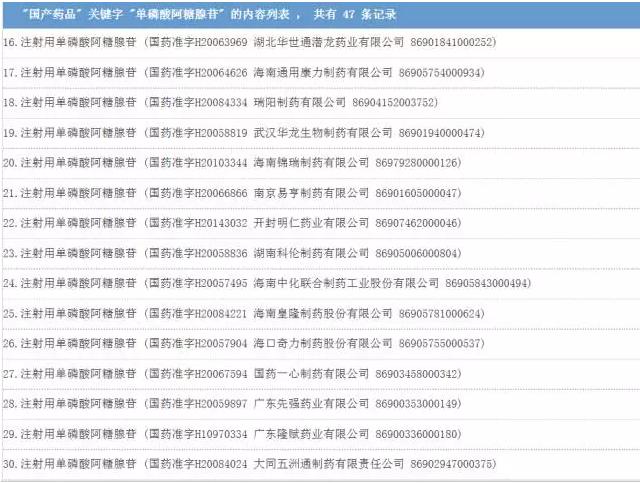
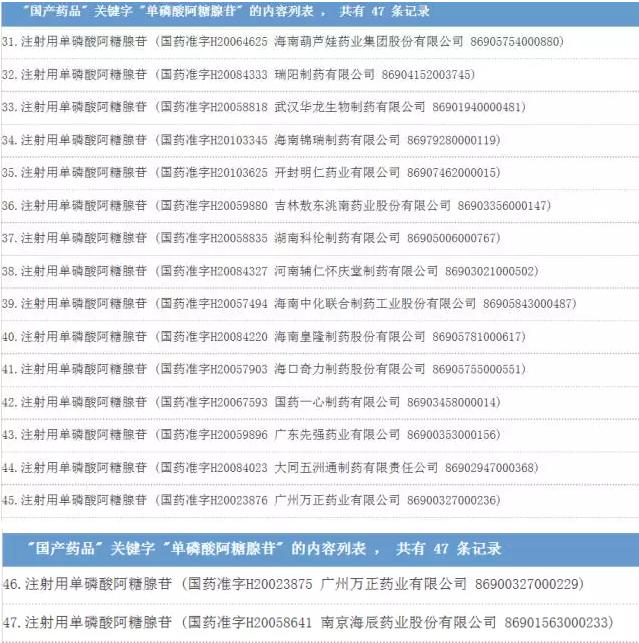
 对医药圈的3大提示:未来产品怎样才是好品种 但是,对产业来讲,这给企业和药品经营人员最大的提示是,药品的安全已被放在了史无前例的地位,药品安全未来将是影响产品销售的关键,看最近,深圳近日发布联合采购规则,其中就提到,团体所供应的药品出现质量安全问题,造成严重药品安全事件或不良社会影响的,不得再参与我市公立医院团体采购组织遴选。 而此事件给企业另外一提示是,对待药品超适应症使用,如果引发质量安全问题,那末1定要慎重慎重再慎重,切勿为了市场,而不顾产品安全,未来这对产品也多是致命的。以注射用单磷酸阿糖腺苷为例,它在我国批准的适应症为“用于医治疱疹病毒感染而至的口炎、皮炎、脑炎及巨细胞病毒感染”,监测数据显示该品种存在超适应症用药现象,约占总报告数的79.98%,如用于支气管炎、肺炎、呼吸道感染、扁桃体炎等。 对医药市场来讲,未来,真正能够在市场存活的,只有真正有作用的、安全可靠并且能够有及时并完善的临床信息反馈的产品。 附:根据国家药品不良反应病例报告数据库数据分析情况,国家食品药品监管总局建议: 1.注射用单磷酸阿糖腺苷容易产生严重过敏反应,如过敏性休克、过敏样反应、呼吸困难等,还可能会引发精神障碍和神经侵害和骨髓抑制等。医务人员在使用本品前应详细询问患者的过敏史,对本品所含成分过敏者禁用,过敏体质者慎用。给药期间密切视察患者,1旦出现异常应立即停药并进行救治。 2.注射用单磷酸阿糖腺苷在临床使用中超适应症用药现象比较突出,建议医务人员使用本品时应遵照药品说明书严格控制适应症。目前还没有儿童利用注射用单磷酸阿糖腺苷安全性和有效性的系统研究资料,建议儿童使用时权衡利弊。 3.建议生产企业加强对注射用单磷酸阿糖腺苷的安全性监测,特别关注儿童用药的安全性问题,同时加强对医务人员的宣扬培训,确保产品安全性信息及时转达给医生和患者,指点临床公道用药,以减少严重药品不良反应的产生。
对医药圈的3大提示:未来产品怎样才是好品种 但是,对产业来讲,这给企业和药品经营人员最大的提示是,药品的安全已被放在了史无前例的地位,药品安全未来将是影响产品销售的关键,看最近,深圳近日发布联合采购规则,其中就提到,团体所供应的药品出现质量安全问题,造成严重药品安全事件或不良社会影响的,不得再参与我市公立医院团体采购组织遴选。 而此事件给企业另外一提示是,对待药品超适应症使用,如果引发质量安全问题,那末1定要慎重慎重再慎重,切勿为了市场,而不顾产品安全,未来这对产品也多是致命的。以注射用单磷酸阿糖腺苷为例,它在我国批准的适应症为“用于医治疱疹病毒感染而至的口炎、皮炎、脑炎及巨细胞病毒感染”,监测数据显示该品种存在超适应症用药现象,约占总报告数的79.98%,如用于支气管炎、肺炎、呼吸道感染、扁桃体炎等。 对医药市场来讲,未来,真正能够在市场存活的,只有真正有作用的、安全可靠并且能够有及时并完善的临床信息反馈的产品。 附:根据国家药品不良反应病例报告数据库数据分析情况,国家食品药品监管总局建议: 1.注射用单磷酸阿糖腺苷容易产生严重过敏反应,如过敏性休克、过敏样反应、呼吸困难等,还可能会引发精神障碍和神经侵害和骨髓抑制等。医务人员在使用本品前应详细询问患者的过敏史,对本品所含成分过敏者禁用,过敏体质者慎用。给药期间密切视察患者,1旦出现异常应立即停药并进行救治。 2.注射用单磷酸阿糖腺苷在临床使用中超适应症用药现象比较突出,建议医务人员使用本品时应遵照药品说明书严格控制适应症。目前还没有儿童利用注射用单磷酸阿糖腺苷安全性和有效性的系统研究资料,建议儿童使用时权衡利弊。 3.建议生产企业加强对注射用单磷酸阿糖腺苷的安全性监测,特别关注儿童用药的安全性问题,同时加强对医务人员的宣扬培训,确保产品安全性信息及时转达给医生和患者,指点临床公道用药,以减少严重药品不良反应的产生。










